【決定版】相対質量・原子量・分子量・式量の定義、求め方、計算問題


25molです。 モル質量とは、その物質が6. >>>大学の数学のテストでlogが出てきた場合は底が10と解釈してよいのでしょうか?? 数学であれば、底がeの対数(自然対数)です。 また、 化学反応を起こす際に必要な物質の質量を求めたり、あるいは物質の質量から個数を求めることが簡単になります。
16

25molです。 モル質量とは、その物質が6. >>>大学の数学のテストでlogが出てきた場合は底が10と解釈してよいのでしょうか?? 数学であれば、底がeの対数(自然対数)です。 また、 化学反応を起こす際に必要な物質の質量を求めたり、あるいは物質の質量から個数を求めることが簡単になります。
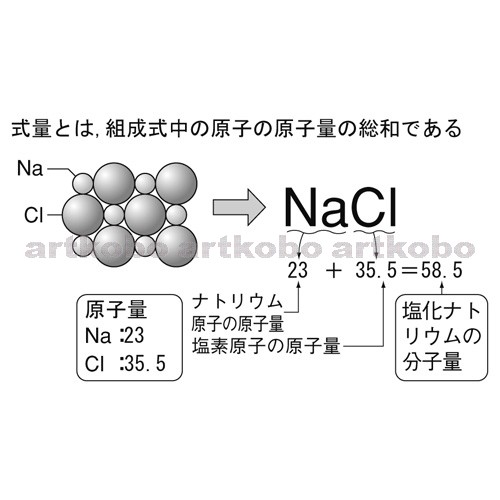
16この中には、C原子が1 mol、O原子が2 mol含まれているので、計算とも合いますね! 式量とは? ここまで、原子の元素ごとの質量数の平均である原子量と、分子の合計の質量数とみなせる分子量について説明をしました。

例えば 111 面とは言いますが 222 面なる表現は使いません。 よって以下が公式です。 空気がこの2種類の分子から構成されていると仮定して、空気の平均分子量を求めなさい。
0 正確にいうと分子量に単位はありません、が 実際の計算では「1 molあたりのグラム数」を表します。 化学の分野ではここまでの精度で取り扱ってもいいだろうという数字です。
) 例えば、塩素には 35Clと 37Clの2種類の同位体が存在します。 よって、 [個] 2 について• まずはこちらからご連絡ください! ポイント• この数字で見ると他にも疑問が出てくるでしょう。
同じように、 原子の1個の重さも 元素 原子の種類 によって違います。 5と整数からかなり外れた値をとります。

だからアボガドロ数を6. (その他の原子の相対質量が気になる場合は、教科書やインターネットを調べれば出てくる) では、この相対質量と原子量の関係を見ていこう。
12【解説・解答】 平均分子量は分子量の平均値です。 0、酸素16なので分子量は180となります。

入試では与えられる数値なので覚える必要はありません。 なぜなら、ハミルトニアンは、実の定数分の不定さがあるからです。
よって、6. もう分かりましたか。 原子量は相対値なので、基本的には単位はありません。