酸


酸化反応でできるものや、プロトンとのイオン結合でできるものがある。 また、酸は多くの人が、酸化力が非常に強い物質と誤解しがちだが、硫酸など一部の例外を除き、酸化力は非常に弱い。 この2つの定義は、記述問題で出ることがあります。
2

酸化反応でできるものや、プロトンとのイオン結合でできるものがある。 また、酸は多くの人が、酸化力が非常に強い物質と誤解しがちだが、硫酸など一部の例外を除き、酸化力は非常に弱い。 この2つの定義は、記述問題で出ることがあります。
2塩基とは、 水素イオンH+を受けとるもの。
また、気体の弱塩基はNH 3しかないので注意しましょう。
ここで扱う実験としては、例えば、身近な物質や塩の水溶液のpH 測定、中和滴定の実験などが考えられる。 というのも、NH 3は分子のどこにもOH -を持っていませんよね。
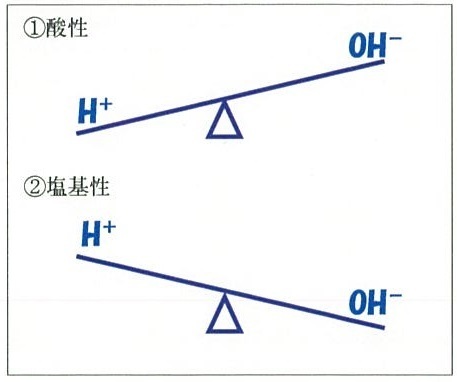

つまり、 水にとかしていないものに関しては、アレニウスの定義では、酸、塩基の決定ができないということです。 清水 訳 2015a. 定義の相対性 [ ] アレニウスの定義と違い、ブレンステッド・ローリーによる酸と塩基の定義は、反応相手となる「他の物質」の存在があって初めて意味を持つものである。 HNO3の電離式は以下の通りです。
ウプサラ大学では、物理学の指導教官に満足できず、化学の指導教官にも満足できなかった。 他にも(の研究)、、、といった方面にも手を出し、間の衝突によってが生まれたとする説を提唱した。

レイアウトなどは引き続き改善していきます。
p K a は定義から数値が小さいほど水素イオンを解離しやすい、すなわち強い酸であることを示す。 スワンテ・アーレニウス『史的に見たる科学的宇宙観の変遷』訳、〈〉、1931年。


晩年の25年間、アレニウスの興味は地学、気象学、宇宙論、さらには免疫学から生物学にまで及び、これらの領域を、当代の物理学と化学、さらにいうならば自らの開拓した理論化学(物理化学)の諸法則により解釈しようとした。 1884年、その研究に基づいて書いた150ページもの学位論文をウプサラ大学に提出。 酸・塩基の定義• 主にの電気伝導率について研究。
11(これは「アレニウスの定義」と呼ばれる。 H 3PO 4• また、eとは自然対数の底であり、近似値は2. 化学基礎 3 物質の変化 イ 化学反応 ア 酸・塩基と中和 中和反応については、酸、塩基の価数と物質量との関係を扱う。
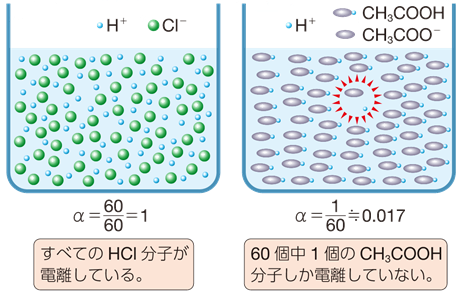
強酸・強塩基の定義 広告 酸・塩基の定義 酸・塩基についての項目は、以下の 5 つのページにまとまっている。 1906年の本ではこの値を1. 濃度を含めた強度 [ ] ある物質の溶液の酸・塩基を議論する際には、その物質の濃度も重要な要素となる。

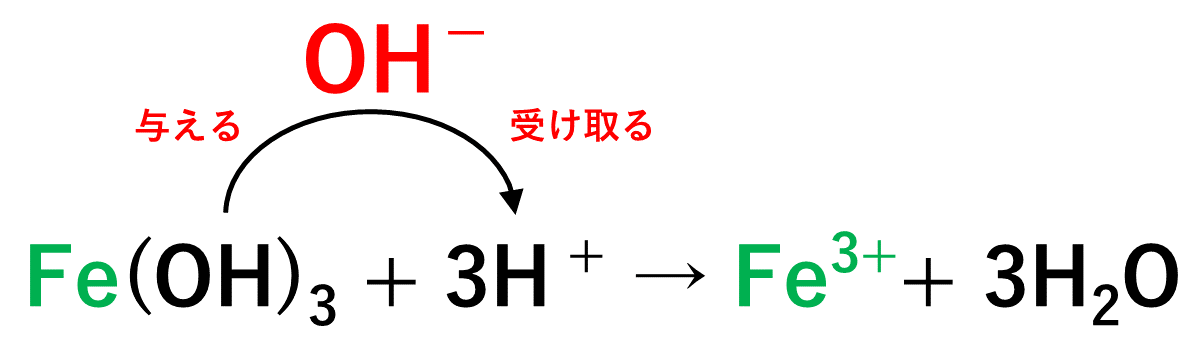
濃塩酸のビーカーの上に、濃アンモニア水に浸したガラス棒を近づけると、ガラス棒から白煙が生じます。 NH 3 はそれ自身が OH - をもっているわけではないが、水と反応して OH - を放出するので塩基に分類される。
6塩基とは、 水溶液中で水酸化物イオンOH -を放出する物質のことです。
+(10-2)+(10-3)+酸と塩基の定義ーアレニウスの定義ー.jpg)

彼は、当時ようやく確立した熱力学の第一法則(エネルギー保存則)、第二法則(エントロピー増大則)と整合性を保つ宇宙論の樹立を企図し、エントロピー減少過程のある星雲の存在を考察したりした。
14アレニウスは、水溶液中では塩がして荷電粒子になると考えた。 気体の塩化水素 HCl とアンモニア NH 3 を反応させると塩化アンモニウム NH 4Cl になります。