単純拡散、促進拡散、能動輸送、膜動輸送
005mMとなりました。 また、消失速度定数や全身クリアランス、分布容積は投与量や血中濃度によらず一定である。 補助因子の中でもは特に重要なものである。
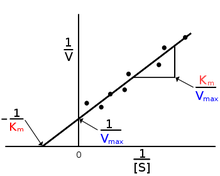
2典型的なEadie-Hofsteeプロット 触媒効率 ある基質に対して作用する異なる酵素の反応速度、または異なる基質に作用する同一の酵素の反応速度を比較するとき、相対的な触媒効率を算出すると、特定の条件下において、どの酵素がどの基質にもっとも適しているのかを知ることができます。 公表されているK iまたはIC 50値が既知の場合は、酵素活性を最大限阻害するため、これらの値の5~10倍高い値を用います。
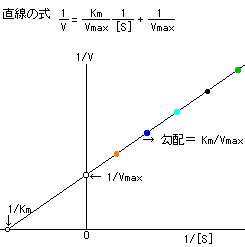
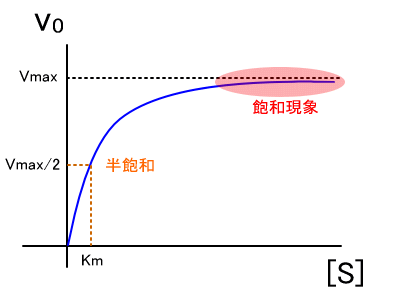
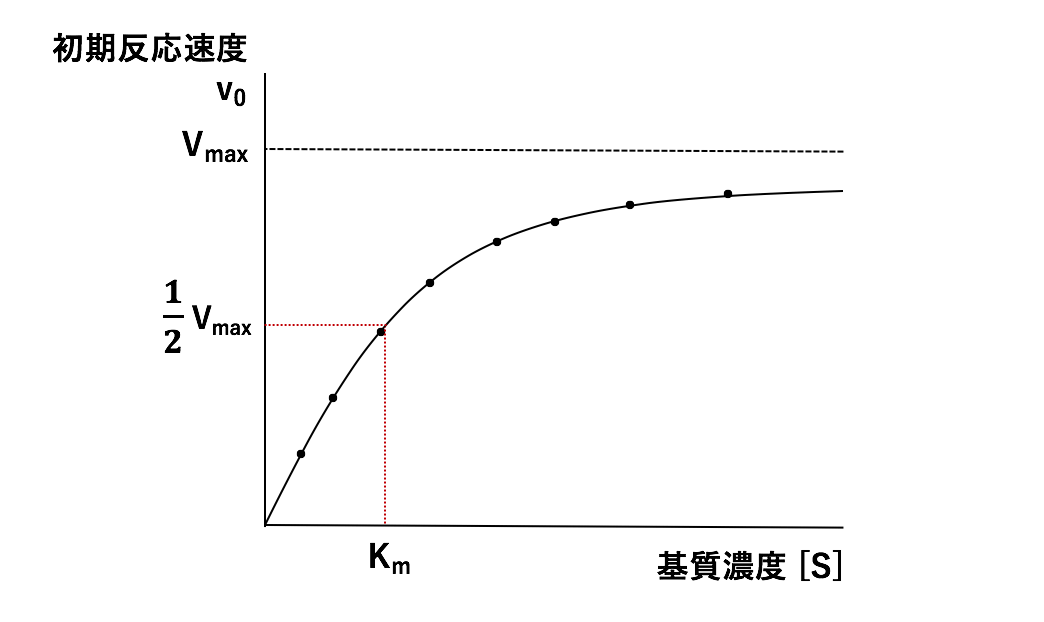
ミカエリス・メンテン式で表される曲線は、ミカエリス・メンテン式によって導かれる近似曲線ですが、このままでは V max値と K m値を求めることはできません(コンピュータを用いれば可能)。
14これらの酵素は複数の結合部位を有しており、阻害剤または活性化因子の結合によって活性が制御されます。 競合阻害 阻害剤の結合部位:基質と同一の酵素の部位(活性中心) Kmの変化:大きくなる Vmaxの変化:変わらない• Sponsored Link まずは、ミカエリス・メンテン式がどのような式であったかを再度確認していきましょう。


バースト相:キモトリプシン CT がCT-酢酸として飽和するまで。 , Kinetics of the reversible inhibition of enzyme-catalysed reactions by tight-binding inhibitors. 酵素反応の進行を妨げることを 阻害といい、これに寄与する化合物を 阻害剤という。
5K iは酵素と阻害剤の親和性の尺度であり、値が小さいほど酵素に対する親和性が強いことを示す。
ある基質Sが酵素Eと反応して生成物Pを得るとき、次の式が成り立つ。
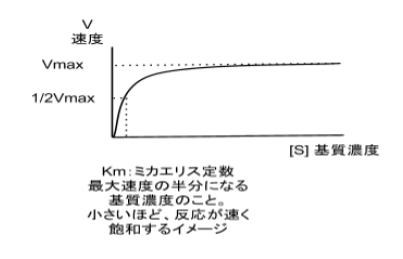
実験的には様々な基質濃度で酵素活性を測定し、横軸に基質濃度、縦軸に酵素活性をとってプロットした場合、図1に示すように、数学的にはの形となる。
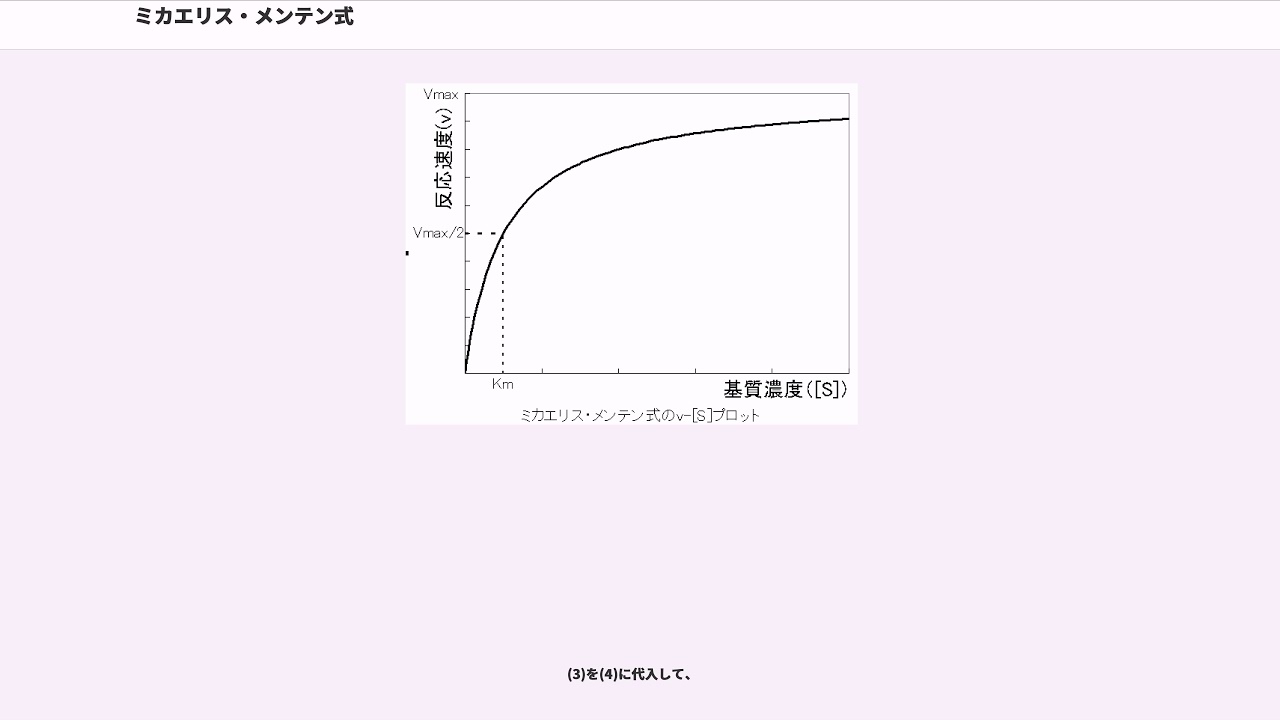
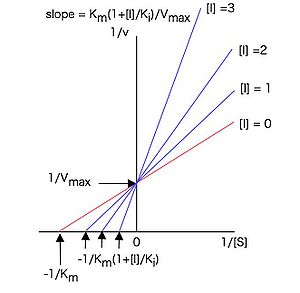
, A linear equation that describes the steady-state kinetics of enzymes and subcellular particles interacting with tightly bound inhibitors. このときVmaxを下げるが、基質の結合自体は阻害しないためKmは変わらない。 複合反応での反応速度 上述のよう量論式から成る化学反応のいくつかを組み合わせた反応のことを複合反応と呼びます。 なお、基質(S)の濃度を[S]と表します。
酵素阻害剤について理解し、利用するには、酵素反応速度論についての基本的な知識が必要です。
Stabilization of calmodulin-dependent protein kinase II through the autoinhibitory domain. 同じ条件なら、ミカエリス・メ. 同様に自己リン酸化部位Thr286周辺の配列を模した合成阻害ペプチドを用いて阻害実験を行うことにより、少なくとも2種類の異なる基質結合部位が存在することが初めて示唆されたが 、この結果は、後に本酵素の活性制御機構やとの相互作用を解明する上で不可欠となるT-site、S-siteという2種類の基質結合部位に関する概念 を確立する上で、先駆的な役割を果たしている。 DFPは、AChEの活性部位におけるセリン残基のヒドロキシル基と共有結合を形成します。 13 式は厳密にはブリッグス・ホールデンの式と言うが、 7 式と同じ形であるので実際にはミカエリス・メンテンの式と言うことが多い。
10参考までに,下のほうに,Hendersonの式を用いて線形解析したデータも載せています。