酸の強さと酸化力について

しかし、亜鉛 Zn を水 H 2 O と反応させると、亜鉛 Zn の表面には、不溶性の水酸化亜鉛 II Zn OH 2 が生じて、内部を保護するため、反応はすぐに止まってしまいます。
17
しかし、亜鉛 Zn を水 H 2 O と反応させると、亜鉛 Zn の表面には、不溶性の水酸化亜鉛 II Zn OH 2 が生じて、内部を保護するため、反応はすぐに止まってしまいます。
170mv~400mvの中間の食品は、それぞれ個人の嗜好もあるので、できるだけ0mvに近い食品を摂取することが大切です。
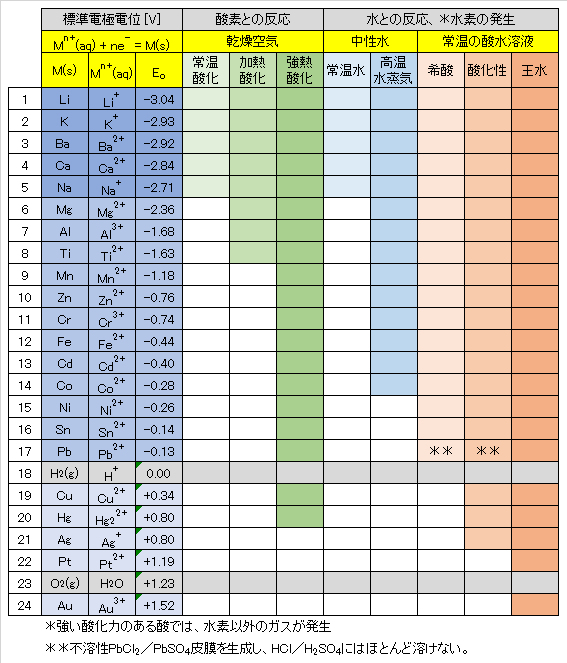
金属のイオン化列と反応性 一般に, イオン化傾向の大きい金属は,反応性が高くなります。 oxidation potntial, electrode potential, reduction potential, redox potentialとも呼ぶ.H 2=2H+2eの反応で(eは電子),電子が水素分子から移動する場合で,すなわち水素が酸化して水素イオンとなる反応を標準とした,相対的な反応のポテンシャルをいう.この反応の酸化ポテンシャル( E oまたは E h)は0 で,他の酸化反応が決められ,酸化還元はを0として計算される.酸化還元ポテンシャルは,反応のおよびによって変化する.pHのような環境の酸化還元ポテンシャルは,の形成や溶液の中に特定のが濃集する要因として重要である[ : 1949]. 出典 岩石学辞典について の解説 電子移動で共役関係にある酸化体と還元体の溶液に、白金板のような不可侵電極(それ自身は酸化還元反応に関与しない不活性な物質の電極)を浸したときに現れる電位で、標準電極電位と同じく標準水素電極との電位差で表す。
もともとは単に酸性が強い水という意味で「超酸化水」や「強酸性水」などと呼ばれていました。

しかも長期にわたって、増大してきます。 。
間接的な関係はある。

ところが、いきなり-82mvの数値です。 この理由は、水に難溶な塩である塩化鉛 II PbCl 2 や硫酸鉛 II PbSO 4 が鉛 Pb の金属表面に生じて、反応がそれ以上進行しなくなるからです。
49 王水と金 Au の反応 さらに、クロム Cr やアルミニウム Al 、鉄 Fe 、コバルト Co 、ニッケル Ni などの三価以上の陽イオンを作る金属は、濃硝酸 HNO 3 のような水 H 2 O の少ない状況下で酸化されると、金属表面に厚さ数 nm 程度の緻密な構造を持つ酸化皮膜が生じて、金属内部を保護するようになります。
そして、フリーラジカルの増加は、ガンや生活習慣病の発症や老化を促進することになります。 ということで、、、溶媒を加えてみました。
反対に還元は電子を受け取ること、と定義されるようになりました。