酸化剤と還元剤|化学基礎【高校化学Net参考書】

イオン結合の物質はイオンの価数で判断。 酸化剤、還元剤どちらともなりうるもの 二酸化硫黄と過酸化水素は、反応の相手が酸化剤なら自身は還元剤として働き、反応の相手が還元剤なら自身は酸化剤として働き、特別なのでその都度どちらなのかを判断してください。
2
イオン結合の物質はイオンの価数で判断。 酸化剤、還元剤どちらともなりうるもの 二酸化硫黄と過酸化水素は、反応の相手が酸化剤なら自身は還元剤として働き、反応の相手が還元剤なら自身は酸化剤として働き、特別なのでその都度どちらなのかを判断してください。
2すなわち,還元されていることになります。 よって,酸化還元反応においては,必ず酸化剤と還元剤が存在します。
消毒に使うオキシドールは,約3%の過酸化水素水溶液です。 答 酸化剤:ヨウ化物イオン 還元剤:塩素 この問題では、酸化剤、還元剤ともにハロゲン(17族)元素が登場しますが、後に無機化学の分野で重要になってきます。


半反応式を導く•。 足りない還元力をブーストさせるのがアルカリ剤って感じすね。 多原子イオンの酸化数 複数の原子で構成されている 多原子イオンも、その価数=酸化数となります。
16注 2)二酸化硫黄は通常は還元剤として働くが,硫化水素などの強い還元剤と反応するときは酸化剤として働く。 酸化還元反応を見分けるシンプルな方法 酸化還元反応かどうかを見極めるには、 【酸化数の変化】に注目します。
非常にわかりにくい。


酸化数とは? 酸化数とは、その名の通り原子の単体がどのくらい酸化されているかをあらわす数値です。 一方,還元剤は化学反応において,反応する相手を還元する(電子を与える)物質のことをいう。
6この場合、酸化数が増加した原子を含むMgが還元剤、酸化数が減少した原子を含むO2が酸化剤ということになります。
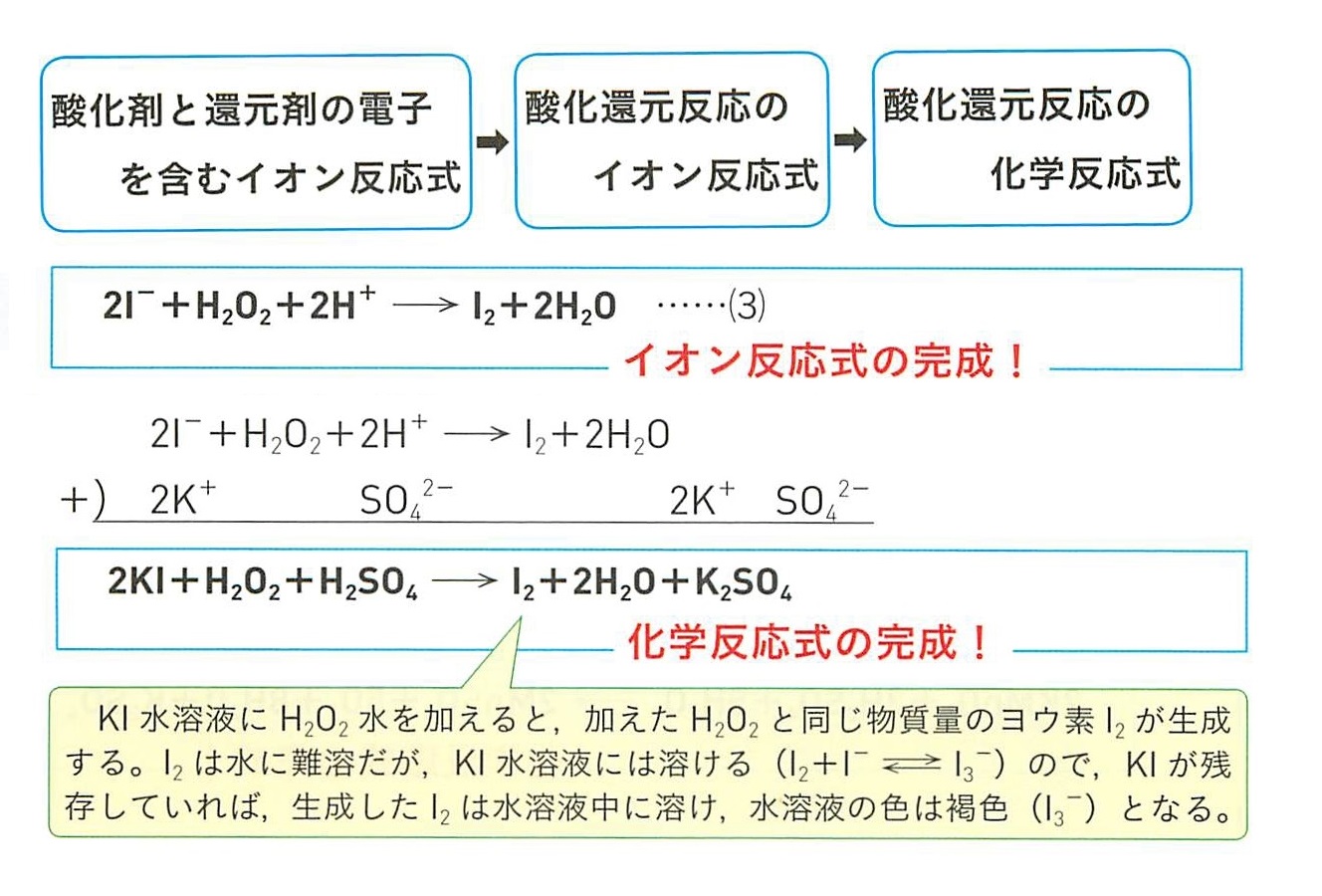

還元作用はアルカリでも中性でも還元作用はあるわけなんです。 少しややこしいですが,がんばってください。 還元 3.1,2の反応では,原子の酸化数はどのように変化しますか? 例として,過マンガン酸カリウム(硫酸を加えて酸性にした水溶液)と過酸化水素の酸化還元反応について,イオン反応式をつくっていきます。
なので酸性染料はいろおちしてくるっつーことすね。 ハロゲンの単体の酸化剤としての強さは, F 2>Cl 2>Br 2>I 2 です。

では、実際に半反応式を書く方法を3つの例(銅濃硝酸シュウ酸 を交えて教えていきます。 化学反応式の中の原子について、酸化数はこのようにして求めます。 酸化剤の意味 酸化剤は、「相手」を「酸化する」もので、「酸化剤自体」は、「還元され」ます。
15アンモニアはアルカリ性の物質。 例外:過酸化水素のOの酸化数はー1 「酸化剤」・「還元剤」の意味と例題 簡単に、酸化剤と還元剤の復習をしておきます。


反応式をつくるときには,気にしなくてよい。 たとえば,銅と希硝酸の反応などは,未定係数法の問題としてよく出題されています。 最後に,酸化数の増減について考えましょう。
7還元されていますね。 だから、役割は迷いません。