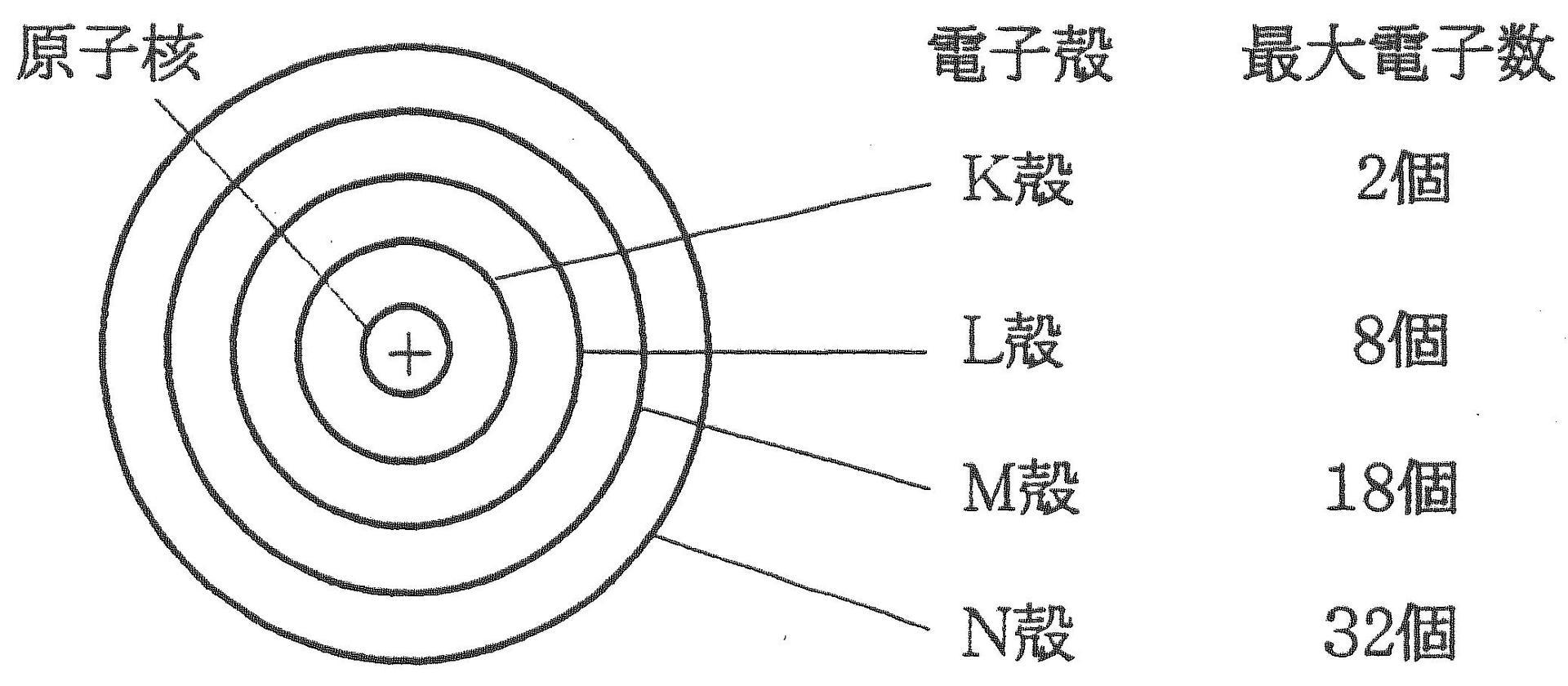
原子の電子配置 電子殻と電子数

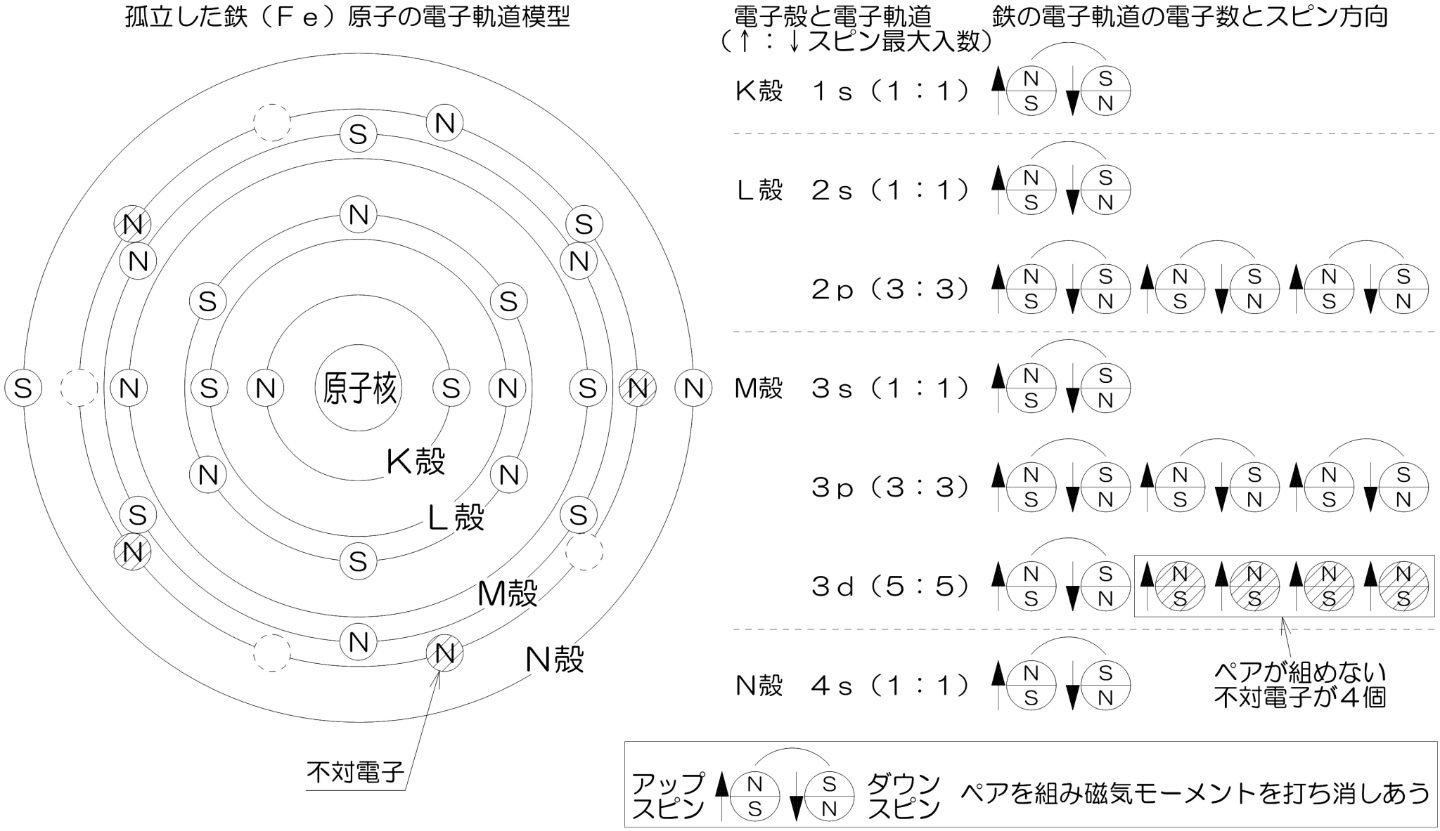
電子は内側の殻から順番に配置される。 今までの疑問も少し晴れたのではないでしょうか。
8s電子 - 上の電子。 こうして6つ全ての電子が詰まりました。
p電子 - 上の電子。 しかし高い電圧をかけてエネルギーが与えられると、電子はL殻、M殻、N殻と外側の電子殻に移動します(左図)。
電子のとり得る軌道は n、 l、 m の3つによって指定される。 4f電子、5f電子が存在する。
第2周期の分子軌道まとめ ここまでは、各分子内の軌道のエネルギーの上下関係にのみ注目していた。 2p電子、3p電子、4p電子、5p電子、6p電子、7p電子が存在する。 「原子」においては,陽子の数=原子番号=電子の数 (イオンでない限り、陽子の数と電子の数は同じです。
10このため、1価の陽になりやすい。

電子配置はそれ自体が入試で問われることは少ないです。 Sc(スカンジウム)やY(イットリウム)では、最外殻電子軌道(4sまたは5s)とその次に外側にある電子軌道(3dまたは4d)に電子が入り、この電子が元素の性質を決めています。
20やと言ったは希ガスに電子を1個追加した配置になっている。
ここでは、 1s 22s 22p 63s 23p 6 が共通式として現れていることが分かります。 すなわち、方位量子数 l が大きくなるほど軌道は原子核から遠くに分布するため、電子間相互作用の影響が大きくなる。
7以上をまとめると下表のようになる。
内殻電子 [編集 ] 最外殻電子()の軌道より内側にあるものは 内殻電子 Core electron と呼ばれる。 具体例1:炭素 6Cの電子配置 原子番号6、すなわち電子数6個の炭素の電子配置をK殻から順番に埋めていきます。
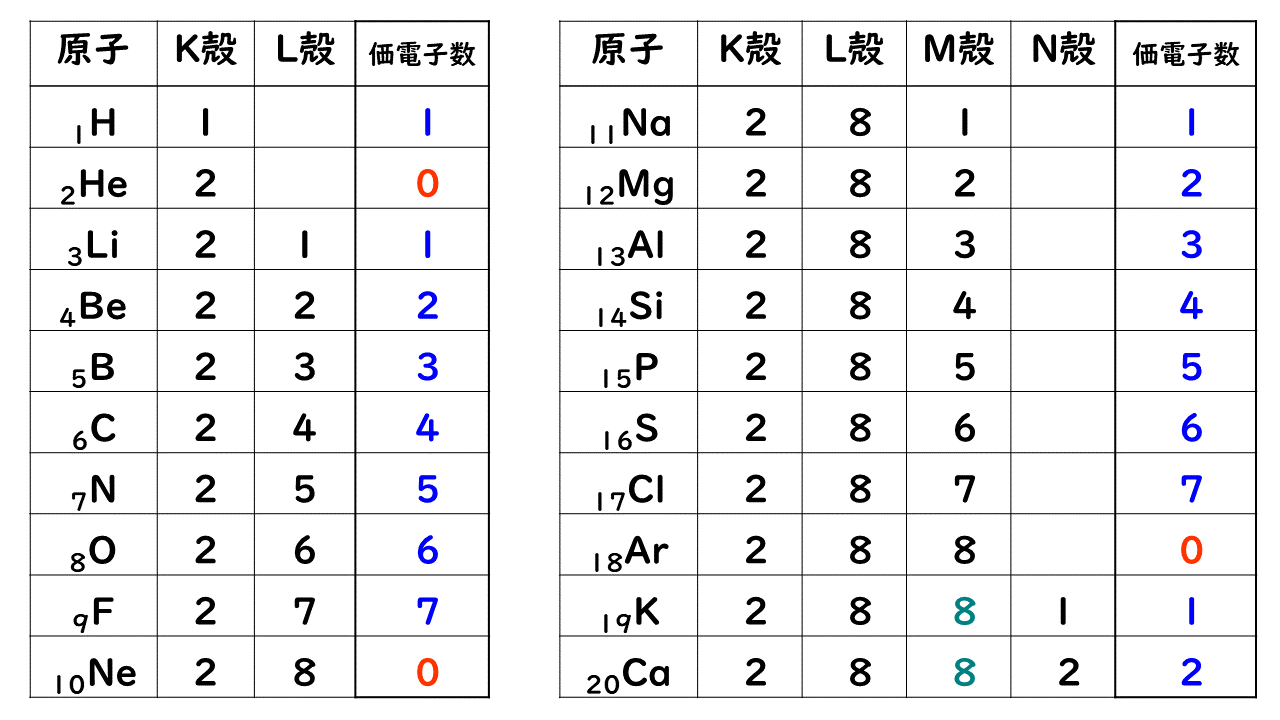

これで窒素の持つ7個の電子全てが収まったので完成。 何度も繰り返し復習して身につけましょう。 M殻に 8個 M殻は18個収納可能ですが、最外殻は8個までと定義されているので18個ではなく8個• 反応に使われる、原子の性質を決める電子のことを価電子と言う。
11まずは最もエネルギーの低い1s軌道に電子が2つ入ります。