イオン化傾向の、よい覚え方ありませんか?ごろあわせ的なもので…よろしくお願いし...


しかし、高校化学では、イオン化傾向の関係を用いて、反応性を考察する問題が多く出題されるので、代表的なものについては、覚えておく必要があります。


しかし、高校化学では、イオン化傾向の関係を用いて、反応性を考察する問題が多く出題されるので、代表的なものについては、覚えておく必要があります。
63Niなどの核放射による方法は、電子 によるイオン化だが、エネルギーによるイオン化でもある。
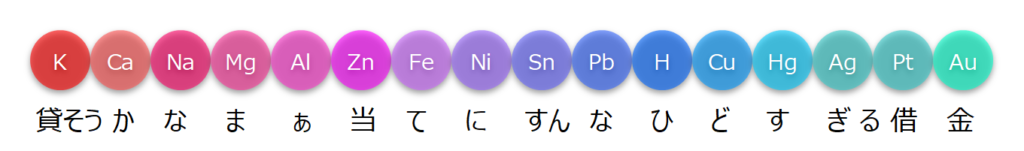

しかし正確には、前述の説明のようにイオン化の容易さではなく、二つの元素のどちらがより酸化され易い(あるいは還元され易い)か、つまり酸化還元反応における化学平衡がどちらに偏っているかの序列である。 ただ、これを全ての原子で覚えるのはまず不可能です。 銀 Ag よりもイオン化傾向が大きい金属 Li ~ Cu は、この反応が進行しません。
7それはに束縛されているがするのに必要なエネルギー値であり、文字通りのイオン化のしやすさの指標である。
イオン化傾向の問題点 [ ] 標準酸化還元電位、ギブス自由エネルギーに基づくイオン化傾向は、イオンの状態をイオン間の相互作用の働かない無限希釈を基準としているため、通常の実験的濃度において必ずしもこの順序が保持されるとは限らず、特に電位の接近しているとなどの順序はあまり意味を成さないとの意見もある。


本題に入る前に、基礎的な知識になるイオンについて確認しましょう。 イオン化傾向が小さいほどイオンは還元され金属として析出しやすくなる。 勉強してもなかなか成果が出ずに悩んでいませんか? tyotto塾では個別指導とオリジナルアプリであなただけの最適な学習目標をご案内いたします。
11次に、「水との反応」についてです。 イオン化傾向を使って解く問題 イオン化傾向は、それ自体を題材にした問題、即ちイオン溶液に金属板を浸す反応について出題されることもあれば、電池の起電力の様に表面的にはイオン化傾向と関係ないように見えるものの、実際はイオン化傾向について問われることもあります。


」 このようにイオン化傾向が大きい金属を、イオン化傾向が小さい金属の溶液に浸すと、電子のやり取りが起きてイオン化傾向が小さい金属が析出します。 だから『会えん鉄道』なのでしょう。
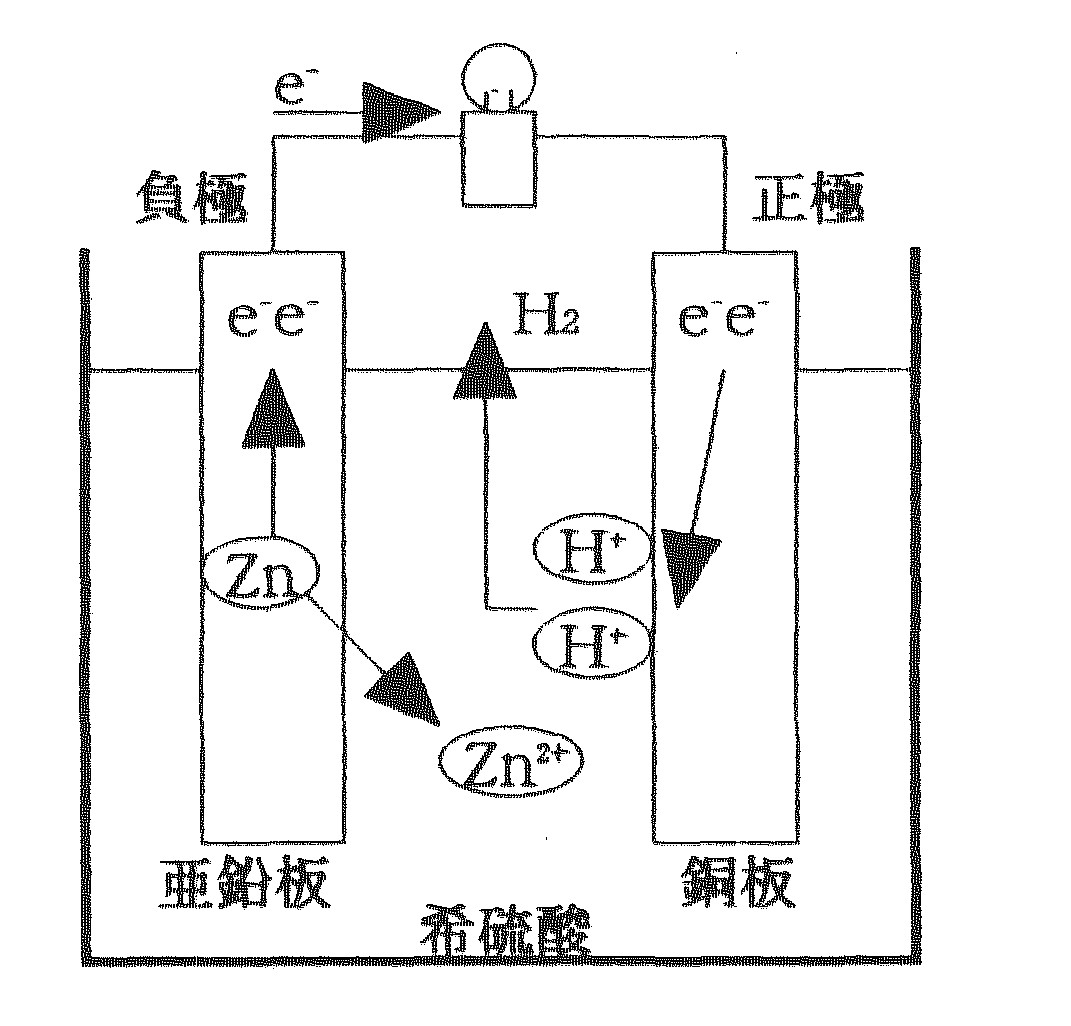
20よく出るのが電池の問題(ボルタ電池)ですね。
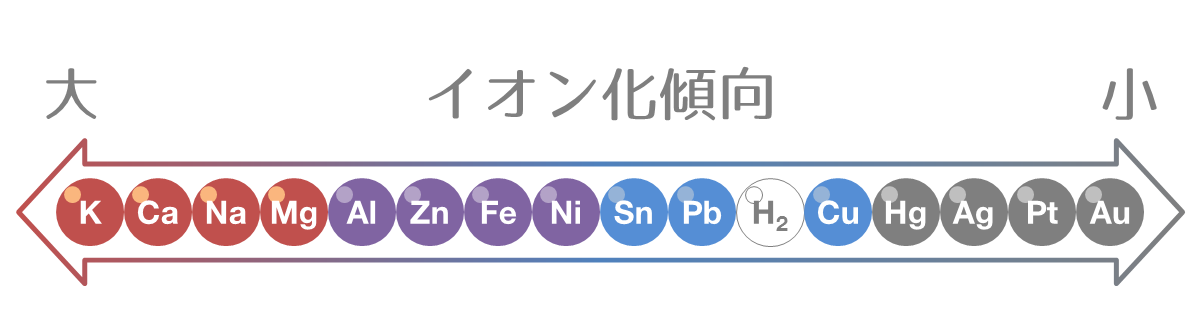
また、ステンレスは、含有するクロム Cr が空気酸化により不動態化したものです。 そのため、イオン化傾向を定義することによってイオンになりやすいかどうかを表しているのです。
15中でもPtやAuは通常の酸化剤とは反応せず、王水と呼ばれる濃塩酸と濃硝酸を3:1で混ぜた非常に強い酸化力を持つ酸化剤としか反応しないことが知られています。 この順でイオン化傾向が大きいのです。
一方、水素は亜鉛によって還元(電子を受け取る)されるため、水素ガス(H 2)を発生する。 イオン化傾向は電気分解、金属と酸の反応、電池などの問題を解くうえでとても重要な基礎になります。
この反応は、イオン化列の鉄 Fe まで起こり、鉄 Fe では逆反応も起こるため、平衡状態となります。


このとき個々の原子は、中性分子のイオン化により電子配置が安定化する現象を、内で実現している。
これをゴロで覚えてしまいましょう。